转折!阿斯利康替格瑞洛的晶型专利无效判决被撤销
 27318
27318
 0
0
 2018/12/30
2018/12/30
2018年12月24日,就阿斯利康公司替格瑞洛化合物发明专利(99815926.3)的专利无效行政诉讼,北京高院作出二审判决,判决撤销北京知识产权法院(2018)京73行初753号行政判决,撤销专利复审委作出的33591号专利无效的行政判决,并要求复审委就原无效宣告请求重新作出审查决定。
阿斯利康的替格瑞洛是第一个三唑并[4,5-D]嘧啶类抗血小板聚集药物,于2011年7月被美国FDA批准上市,2012年11月获得我国食药监局颁发的进口药品许可证,正式进入中国市场。与其主要竞争对手氯吡格雷相比,替格瑞洛不需要经过肝脏代谢激活,具有更快速、更强效抑制血小板的特点。自上市以来,替格瑞洛已被多部欧美指南推荐为ACS患者的一线或首选抗血小板药物,其销售额也不断攀升,2016年全球销售额已达到8.39亿美元,有望跨入“重磅炸弹”俱乐部。
在替格瑞洛的众多仿制药申报者中,深圳信立泰拔得了头筹。在率先完成生物等效性实验后,信立泰于今年3月9日第一个提交了上市申请。在11月22日CDE公布的名单中,信立泰的替格瑞洛片又被纳入了优先审评程序。可见,信立泰已经基本上扫平了药品注册道路上的障碍,坐等成为替格瑞洛的首仿厂家。
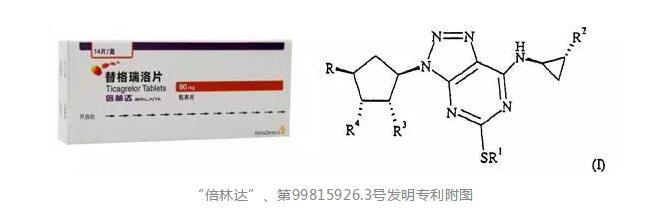
“倍林达”、第99815926.3号发明专利附图
2017年4月27日,深圳信立泰药业股份有限公司(下称信立泰公司)针对第99815926.3号发明专利提起无效宣告请求,并提交了7份证据,其中证据1为WO98/28300A1专利文献,公开日为1998年7月2日。
除了针对“替格瑞洛”的化合物专利发起无效宣告请求之外,信立泰公司亦将“矛头”指向了该药物的晶型专利。2017年10月16日,双方针对第200610002509.5 “三唑并[4,5-D]嘧啶化合物的新晶形和非晶形”专利,举行了口审。在此之前,南京华讯知识产权顾问有限公司针对该专利发起了两次无效宣告请求。
2018年12月24日,就阿斯利康公司替格瑞洛化合物发明专利(99815926.3)的专利无效行政诉讼,北京高院作出二审判决,判决撤销北京知识产权法院(2018)京73行初753号行政判决,撤销专利复审委作出的33591号专利无效的行政判决,并要求复审委就原无效宣告请求重新作出审查决定。
“交战”时间轴
2017年4月27日,深圳信立泰率先发起专利挑战,以不具备创造性为由,向专利复审委请求宣告99815926.3号专利全部无效。
2017年10月17日,专利复审委作出33591号专利无效审查决定,宣告该化合物专利全部无效。
2018年1月16日,阿斯利康正式向北京知识产权法院提起诉讼,请求撤销专利复审委的无效决定,并请求判令其重新作出审查决定。
2018年7月30日,北京知识产权法院认为,本专利权利要求1相对于证据1和公知常识的结合,不具有突出的实质性特点和显著进步,因此不具备创造性,判决驳回阿斯利康公司的诉讼请求。
2018年8月30日,阿斯利康向北京高院提起上诉。
2018年12月24日,北京高院作出二审判决,认为原审判决及被诉决定部分事实认定不清,适用法律错误,依法均应当予以撤销,专利复审委应就该专利的无效宣告请求重新作出审查决定。
0






热门评论